Quando se entra em contato com um agente infeccioso, o que frequentemente também leva à destruição de tecidos, o sistema imune é ativado. Recentemente, tem sido bastante estudado a ideia de que, quando uma bactéria invade o organismo, a resposta imune trabalha no sentido de tentar eliminar esse patógeno, impedindo que ele se prolifere muito, mas também atua para fazer o reparo desse tecido danificado. O laboratório da professora Maria Regina D'Império Lima, do Instituto de Ciências Biomédicas (ICB) da USP, estuda a resposta imune ao dano celular na tuberculose e descobriu, recentemente, que sinalizadores dessas lesões induzem a morte de células de defesa, influenciando na proliferação da doença.
M. tuberculosis: bactéria resistente
A tuberculose é uma das doenças mais antigas de que se tem conhecimento e, apesar dos muitos avanços na área, ainda é um problema de saúde pública. A infecção, causada pela bactéria Mycobacterium tuberculosis, acontece por vias respiratórias. "Em geral, ela vai para o pulmão, onde se instala no tecido pulmonar", explica a professora Maria Regina D'Império Lima. Esse microrganismo é muito persistente; o sistema imune tem grande dificuldade de eliminá-lo completamente e o mantém numa estrutura envolvido por células de defesa, o granuloma, impedindo que se multiplique. "A bactéria não morre, mas fica presa por essa estrutura", afirma Regina.
Na grande maioria dos casos, a infecção permanece nesse estágio dormente, em que a pessoa tem a bactéria mas não desenvolve a doença. Porém, esse agente infeccioso pode começar a crescer muito dentro do granuloma de modo que o organismo não consegue mais prendê-lo – ele se espalha e, então, instala-se a tuberculose. "A bactéria se distribui pelos tecidos e passa a ser infectante. A pessoa está cheia delas; se ela tossir, por exemplo, outra pessoa pode ser infectada", diz a professora. As micobactérias conseguem romper essa estrutura de defesa, mantida no interior de células do sistema imune chamadas macrófagos, desencadeando uma forma violenta de morte – a necrose. Com a morte dos macrófagos, o conteúdo se espalha e há uma grande destruição de tecidos.
Vários motivos podem levar essa passagem da infecção latente para a tuberculose de fato, explica Regina. Isso pode ser determinado por características genéticas individuais ou à queda da imunidade – por estresse físico ou psicológico ou por doenças como a aids. "O paciente com aids tem uma queda na resistência; quando isso acontece, o organismo encontra-se vulnerável à tuberculose", comenta.
Sinalizadores de lesão celular
Esse processo desordenado de morte dos macrófagos dispara no tecido uma série de sinalizadores do dano celular. Por um lado, essa sinalização é importante e saudável ao organismo porque atrai mais células de defesa para a região do dano inicial. Mas o excesso dessas moléculas acaba contribuindo para o processo de destruição do próprio tecido, ao iniciar um ciclo de infecção e destruição de macrófagos, levando a um processo inflamatório generalizado, segundo estudo do laboratório do ICB.
Um desses sinalizadores é a molécula de trifostato de adenosina, o ATP. Por ser um importante armazenamento de energia, o ATP está presente em grande quantidade nas mitocôndrias, dentro da célula. "Normalmente existe muito ATP no meio intracelular e pouco fora dele", aponta a professora. Mas, quando a célula se rompe, pelo processo de necrose, essas moléculas saem da célula. Esse ATP e substâncias decorrentes de sua degradação podem ser reconhecidos por células que estão ao redor por meio de receptores chamados receptores purinérgicos. "Eles avisam que existe ATP ou seus subprodutos do lado de fora da célula e isso pode ter diferentes consequências para a resposta imune", afirma Regina. O trabalho realizado no laboratório do ICB mostrou que a ativação desses receptores induz a morte celular.
A morte de uma célula infectada por uma bactéria, apesar do dano causado, pode ter consequências desejáveis. “O patógeno que estava crescendo dentro dela pode também ser destruído”, destaca Regina. Porém, no caso da tuberculose, bactérias de algumas cepas consideradas hipervirulentas são tão resistentes que não morrem junto com a célula; elas conseguem sobreviver e se espalhar. “Essas cepas têm uma casca, uma parede celular muito forte e difícil de ser destruída”, acrescenta.
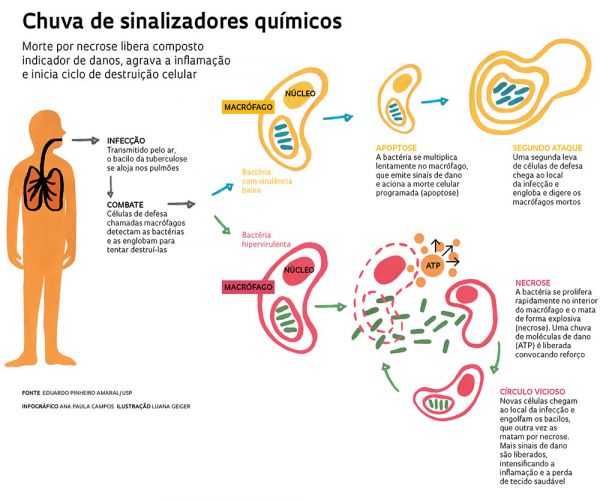
Morte por necrose libera composto indicador de danos e agrava inflamação (Infográfico: Ana Paula Campos/Ilustração: Luana Geiger, para Revista Pesquisa FAPESP, ed. 222)
O que acontece, explica Regina, é que, quando a bactéria da tuberculose cresce descontroladamente e rompe a estrutura de defesa criada pelo sistema imune, instalando-se a doença, a célula morre, causando um grande dano, e uma série de moléculas de ATP é eliminada para o meio extracelular. As moléculas de ATP são reconhecidas por esses receptores, que induzem a morte de mais células, causando mais dano. Como a bactéria é resistente, ela não morre no processo de necrose e se espalha por outros tecidos, onde o mesmo processo vai acontecer mais uma vez: o granuloma vai se formar, as bactérias vão crescer e, depois, essa estrutura vai ser destruída, liberando mais moléculas de ATP que serão reconhecidas pelos receptores purinérgicos e levarão à morte celular.
Um dos receptores de ATP estudados no laboratório do ICB para confirmar essa situação é chamado de P2X7. Dois tipos de camundongos – um deles normal com o receptor P2X7 e outro modificado para não ter a molécula – foram infectados com cepas hipervirulentas de M. tuberculosis que induzem o processo de necrose. Os animais sem o P2X7 estavam muito mais protegidos do que os que tinham a estrutura, o que mostra que o receptor de ATP contribui para a morte do macrófago.
Tratamento em conjunto com antibióticos
O estudo, além de ajudar na compreensão do processo de como essas bactérias agem, sugere possibilidades de utilizar bloqueadores de P2X7, que impedem a sua ativação, para tentar fazer com que a doença seja mais branda. A intenção, esclarece a professora, não é utilizar isso como uma terapia única, porque o que se usa hoje em dia no tratamento da tuberculose, os antibióticos, funcionam bem. “Somando mais um conceito, que não só tentasse destruir as bactérias, mas que também impedisse o dano celular, a eficácia pode ser maior”, afirma Regina.
Na aids, principalmente, pelo uso excessivo de antibióticos que o indivíduo imunosuprimido deve tomar para se tratar, há indicações de que está aumentando a quantidade de bactérias com maior capacidade de se multiplicar. Por isso, além de abrandar a tuberculose e oferecer mais tempo para o tratamento dos pacientes, o bloqueio do receptor é uma alternativa importante ao problema dessas bactérias hipervirulentas e de patógenos que têm se tornado resistentes aos antibióticos.