|
| |
| NESTA EDIÇÃO |
| |

|
O
governador Geraldo Alckmin lembrou os tempos de infância ao
anunciar, no dia 15 passado, em cerimônia no Palácio
dos Bandeirantes, a conclusão do mapeamento genético
do Schistosoma mansoni, causador da esquistossomose – popularmente
conhecida como “barriga d’água”. “Quando
eu era criança, meu pai, que era veterinário, resolveu
pesquisar como algumas espécies de peixes poderiam ser usadas
para combater os caramujos que causam a esquistossomose”,
disse o governador, destacando a “grande importância”
da mais recente façanha da ciência paulista. O anúncio
foi feito com a presença do secretário estadual de
Ciência e Tecnologia, João Carlos Meirelles, do reitor
da USP, Adolpho José Melfi, do presidente do Conselho Superior
da Fapesp, Carlos Vogt, e do diretor-científico da Fapesp,
José Fernando Perez. O projeto
de mapeamento genético do Schistosoma mansoni teve a participação
de 37 pesquisadores ligados a nove laboratórios da USP, Unicamp,
Instituto Butantan e Instituto Adolpho Lutz. Iniciada em junho de
2001, a pesquisa foi coordenada pelo professor Sérgio Verjovski
Almeida, do Instituto de Química da USP e custou US$ 1 milhão,
divididos igualmente entre a Fapesp e o Ministério da Ciência
e Tecnologia. Os resultados divulgados por Alckmin estão
publicados na edição de outubro da revista Nature
Genetics, lançada no mesmo dia 15 de setembro, sob o título
Transcriptome analysis of the acoelomate human parasite Schistosoma
mansoni. Mais
do que um grande feito científico – comparável
ao célebre mapeamento da bactéria Xylella fastidiosa,
causadora da praga do amarelinho, também realizado nos laboratórios
paulistas, em 2000 –, o seqüenciamento do DNA do Schistosoma
mansoni representa um passo importante em favor da saúde
pública no Brasil e no mundo. A partir dele, os cientistas
podem investigar agora novas alternativas de tratamento –
incluindo vacinas – da esquistossomose. Não
é pouca coisa. De acordo com dados divulgados pela Fapesp,
a esquistossomose atinge 75 países, a maioria deles situada
em regiões subdesenvolvidas. Cerca de 200 milhões
de pessoas são infectadas a cada ano entre as 600 milhões
que se encontram em situação de risco de contrair
a doença. Do total de infectados, pelo menos 10% ficam gravemente
doentes. O índice anual de mortes causadas pela esquistossomose
no mundo é de 300 mil a 500 mil. “Em termos de impacto
socioeconômico e de saúde pública, a doença
é superada apenas pela malária nos países onde
é endêmica”, informa a Fapesp.
Novos
genes – O término da pesquisa abre novas perspectivas
para eliminar os males causados pela esquistossomose – através
da ciência. Isso porque os pesquisadores paulistas descobriram
um punhado de genes que podem estar relacionados com a doença.
Segundo a Fapesp, o artigo publicado na Nature Genetics aponta 45
novos genes que poderão ser importantes para o desenvolvimento
de drogas e outros 28 que possivelmente estarão na base da
produção de novas vacinas. “A
pesquisa ampliou o número de genes completamente conhecidos
do Schistosoma mansoni de 160 para 510, além de encontrar
outros 14 mil novos genes, o que equivale a mais de 90% do material
genético que codifica as proteínas do parasita. Para
a identificação desses genes foram produzidas 180
mil seqüências de fragmentos de genes expressos, 50%
acima da meta inicial”, segundo a Fapesp. Essas
seqüências são geradas a partir do RNA mensageiro,
molécula que põe em ação as informações
contidas no DNA e dá início à produção
de proteínas na célula. Por isso, elas são
capazes de mostrar quais genes estão mesmo ativos. “Uma
estratégia genômica pode ser tão importante
para combater uma doença típica do Terceiro Mundo
quanto a educação e a prevenção”,
analisa Verjovski. Outros
55% de genes totalmente novos identificados – que não
têm similaridade com genes já seqüenciados de
outros organismos – devem desempenhar funções
biológicas específicas desse tipo de parasita. Isso
amplia as perspectivas do estudo de genes de interesse para o controle
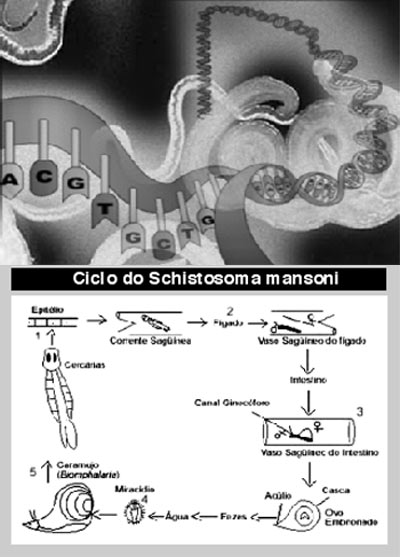
da doença. Ovos
e larvas – O ciclo do Schistosoma mansoni começa com
os ovos do parasita presentes nas fezes de uma pessoa infectada
que vão parar na água. Os ovos germinam e eclodem,
liberando uma larva conhecida como miriacídio. Essa larva
penetra no caramujo do gênero Biomphalaria, multiplica-se
por aproximadamente 30 dias e transforma-se numa segunda larva,
a cercaria. Em apenas um dia, um caramujo libera milhares de cercarias,
que sobrevivem por algumas horas. Nesse período, elas buscam
o homem, seu hospedeiro definitivo. Na
corrente sangüínea ou na linfática, as larvas
chegam aos pulmões, no primeiro dia, e ao fígado,
nove dias mais tarde. Elas se alimentam de sangue e, no vigésimo
dia, tornam-se adultas e começam a se reproduzir. Quarenta
dias depois da contaminação, as fezes do doente já
estão cheias de ovos do Schistosoma mansoni e o ciclo recomeça.
Os principais sintomas da doença são dor de cabeça,
febre, falta de apetite, fraqueza, calafrios e diarréia.
O fígado e o baço incham por causa das infecções,
razão por que é conhecida como barriga d’água. O único
medicamento utilizado no combate ao parasita existente no mercado,
o Praziquantel, é incapaz de impedir que as pessoas sejam
reinfectadas pelo verme, uma vez que gerou linhagens resistentes
desse organismo. Por isso a esperança dos pesquisadores é
poder manipular características específicas do Schistosoma
para criar novos medicamentos e vacinas. Todas
as descobertas realizadas através do estudo são muito
promissoras. Quatro dos genes identificados sintetizam toxinas secretadas
pelo parasita, que se assemelham a quatro tipos diferentes de venenos
de abelha causadores de resposta alérgica. O fato de o Schistosoma
mansoni secretar toxinas alergênicas similares às de
abelhas explica um fenômeno que se sabia estar presente na
doença: a resposta imune do tipo alérgico induzida
pelo parasita.
Os
pesquisadores acreditam que a reação alérgica
a essas toxinas seja uma maneira utilizada pelo parasita de despistar
o sistema imune. Ao intensificar a resposta alérgica, ele
evita a resposta imune de defesa que poderia matá-lo. Espera-se
que o conhecimento dessa arma usada pelo parasita – as quatro
toxinas – permita interferir no mecanismo de defesa e dificultar,
ou impedir, a sobrevida do Schistosoma mansoni na circulação
do homem. Outra
toxina secretada pelo parasita que foi identificada no estudo é
semelhante a uma toxina anticoagulante presente no veneno de serpentes.
Isso revela um mecanismo que provavelmente permite ao parasita viver
na circulação do homem sem ser identificado como corpo
estranho. Espera-se que a partir de um estudo dessa toxina possa
se desenvolver uma vacina que interrompa o mecanismo. Como
forma de proteção intelectual, a Fapesp já
solicitou um pedido de patente internacional para utilização
de genes mais promissores. Com essa proteção, a Fapesp
quer atrair investimentos necessários para os testes que
levem ao desenvolvimento de medicamentos efetivos contra a doença.
|
O Jornal da USP é um órgão da Universidade de São Paulo, publicado pela Divisão de Mídias Impressas da Coordenadoria de Comunicação Social da USP.
[EXPEDIENTE] [EMAIL]