| NESTA EDIÇÃO |
| |
|
Apesar de ser ainda bastante recente – foi publicado em 1998 –, o trabalho dos americanos Andrew Fire e Craig Mello, vencedores do Prêmio Nobel de Medicina de 2006, vem sendo usado intensamente por laboratórios e pesquisadores no mundo inteiro, inclusive na USP. A descoberta que levou à conquista do prêmio, chamada de interferência de RNA, desvenda um mecanismo capaz de abafar a expressão dos genes, e pode representar um caminho no tratamento de enfermidades como câncer, Aids e algumas doenças genéticas. “A técnica é muito poderosa e tem um impacto muito amplo porque permite desligar genes específicos. É uma ferramenta já incorporada como instrumento da pesquisa básica”, destaca a professora Lygia da Veiga Pereira, do Centro de Estudos do Genoma Humano do Instituto de Biociências da USP. Os ganhadores do Nobel deste ano “descobriram um mecanismo fundamental para controlar o fluxo de informação genética”, de acordo com o anúncio divulgado pela Fundação Nobel no dia 2. O genoma opera enviando instruções para a fabricação de proteínas do DNA, no núcleo da célula, para o mecanismo de síntese protéica, no citoplasma, através do chamado RNA mensageiro. A interferência de RNA destrói o RNA mensageiro, impedindo a síntese de proteínas – o efeito, na prática, é semelhante ao “desligamento” do DNA. “Conhecer os genes não significa saber o que eles fazem”, declarou à imprensa o cientista Andrew Fire. É por isso que, na era pós-seqüenciamento do genoma, o grande desafio é entender a função de cada um. “Uma forma de fazer isso é desligar esse gene e verificar quais as conseqüências”, diz a pesquisadora Lygia da Veiga Pereira. Ao disponibilizar uma ferramenta capaz de fazer isso, a interferência de RNA pode ajudar a desvendar a utilidade de dezenas de milhares de genes cujas funções são desconhecidas. A promessa, afirma Lygia, é que esse método venha a ser utilizado no desenvolvimento de terapias para atacar várias doenças. “Essas aplicações estão sendo pesquisadas em laboratório, com resultados muito promissores”, diz. Terapia vascular – Na USP, um dos trabalhos que utilizam a técnica descoberta por Fire e Mello é desenvolvido pela bióloga Luciana Vasques, pesquisadora que faz pós-doutorado no Instituto do Coração (Incor), ligado à Faculdade de Medicina da USP. Seu trabalho integra um estudo em terapia vascular liderado pelo professor José Eduardo Krieger e tem como objetivo diminuir a proliferação celular em pacientes que receberam ponte de safena. Nesse tipo de cirurgia, a veia safena é retirada da perna e colocada numa função arterial para fazer a revascularização do coração. Devido a essa mudança de ambiente, o vaso passa por um remodelamento para “imitar” a função da artéria. Em alguns casos, pode ocorrer um espessamento do vaso, causando a sua oclusão. “A idéia do projeto é diminuir a proliferação de células no vaso para que não ocorra a oclusão”, explica Luciana.
A pesquisadora desenvolveu um RNA interferente contra o gene E2F1, que controla a expressão de genes envolvidos com proliferação celular. Diminuindo-se a expressão desse gene, é possível diminuir essa multiplicação. Em culturas de laboratório, Luciana já conseguiu reduzir a proliferação em 70% e se prepara para o próximo passo, que é aplicar a terapia em modelo animal. “O interessante dessa descoberta é que ela serve para a desativação de muitos genes”, diz a pesquisadora, que fez mestrado e doutorado no Instituto de Biociências da USP, sob orientação de Lygia Pereira. “Esse mesmo gene que estou estudando pode ser utilizado como terapia para outras doenças que envolvem proliferação celular, como câncer.” Importância – “A interferência de RNA ocorre em plantas, animais e humanos. É de grande importância para a regulação da expressão genética, participa da defesa contra infecções virais e mantém sob controle os ‘genes saltadores’”, diz a declaração de anúncio do prêmio a Fire e Mello. “A interferência de RNA já está sendo utilizada como um método para estudar a função de genes e pode proporcionar novas terapias no futuro.” O Prêmio Nobel costuma ser outorgado décadas depois de uma descoberta. Mas, para Bertil Fredholm, integrante da Assembléia do Nobel do Instituto Karolinska, na Suécia, a escolha de Mello e Fire deveu-se à evidente importância da descoberta deles, pois a técnica da interferência de RNA, segundo declarações que deu à imprensa, “invadiu” laboratórios do mundo inteiro. A indústria farmacêutica também vem utilizando o método intensivamente em suas pesquisas, ressaltou. Os pesquisadores americanos estão entre os mais jovens da história recente a receber o prêmio de 10 milhões de coroas suecas (cerca de US$ 1,37 milhão) concedido pela Fundação Nobel. Andrew Fire nasceu na Califórnia em 1959 e é professor na Universidade de Medicina de Stanford. Craig Mello, nascido em 1960, leciona biologia em Harvard. Seu bisavô paterno é um imigrante da ilha de São Miguel, nos Açores. O cientista cresceu fascinado com as origens da vida por ter desenterrado ossos de dinossauro no oeste dos Estados Unidos com o pai, que era paleontólogo. Mello declarou à imprensa que imaginava que seu trabalho pudesse ser premiado, mas só daqui a dez ou vinte anos. |
|
Pai e filho premiados
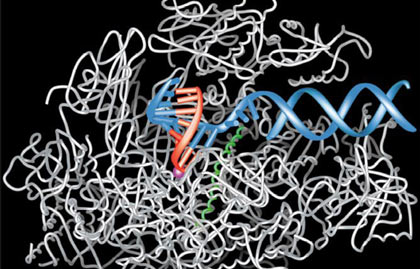
O Prêmio Nobel de Química, anunciado no dia 4, estabeleceu uma linhagem de pai e filho entre dois ganhadores. O agraciado de 2006, o americano Roger Kornberg, tinha 12 anos de idade quando viu seu pai, Arthur, receber a distinção na área de Medicina em 1959. Enquanto o pai descreveu como a informação genética se transfere de uma molécula de DNA para outra, o que o filho fez foi “descrever como a informação genética é copiada do DNA para o que se conhece como RNA-mensageiro”, de acordo com o comunicado da Fundação Nobel. O prêmio de Química deste ano consagra o trabalho de um cientista dedicado à pesquisa genética, assim como o de Medicina. Para que nosso organismo possa utilizar a informação armazenada nos genes, uma cópia precisa ser feita e transferida para partes exteriores das células. Lá a cópia é usada como uma instrução para a produção de proteína – e são as proteínas, por sua vez, que realmente definem a função do organismo. Esse processo de cópia é chamado de transcrição, e Roger Kornberg foi o primeiro a criar uma imagem acurada de como a transcrição funciona no nível molecular em organismos com células eucarióticas (células cujo núcleo possui uma membrana que o separa do citoplasma). Nesse grupo estão incluídos desde grandes mamíferos como os seres humanos a organismos menores como fungos. Os quadros desenvolvidos por Kornberg permitem a observação de um ramo de RNA se desenvolvendo e o papel de várias outras moléculas necessárias para o processo de transcrição. Tão detalhadas são as imagens, define a Fundação Nobel, que “átomos separados podem ser distinguidos, e isto torna possível entender os mecanismos de transcrição e como ela é regulada”. Kornberg, de 59 anos, é doutor pela Universidade de Stanford, onde também é catedrático de Medicina.
|
O Jornal da USP é um órgão da Universidade de São Paulo, publicado pela Divisão de Mídias Impressas da Coordenadoria de Comunicação Social da USP.
[EXPEDIENTE] [EMAIL]