| NESTA EDIÇÃO |
Para que um portador do vírus HIV possa levar uma vida mais longa e saudável, ele deve se tratar com um coquetel de variados medicamentos. Isso exige dedicação e rígida organização e é a maior causa do alto índice de desistência do tratamento, que no ano 2000 alcançou 70% dos pacientes do Estado de São Paulo, de acordo com o Núcleo de Estudos para Prevenção da Aids (Nepaids) da USP. Foi pensando nesse público que o pesquisador Luiz Marcos de Lira Faria, do Laboratório de Eletroativos do Instituto de Química da USP, resolveu desenvolver, em sua tese de doutorado, um sistema-modelo de liberação controlada de drogas. Assim, o coquetel contra a Aids pode ser substituído por um aplicativo automático, adesivo ou subcutâneo, quase invisível aos olhos e imperceptível na rotina dos pacientes. Em cinco anos de pesquisa, o professor desenvolveu um sistema composto de materiais biocompatíveis, que não reagem com as células sanguíneas, evitando reações adversas. O pequeno sistema, de 0,7 por 0,5 centímetros, é formado por uma matriz de hidrogel – um material poroso, transparente, similar a uma gelatina e composto por 80% a 90% de água. “Como nossa idéia é fazer um dispositivo que fique no organismo do paciente, precisamos de um material que não o agrida. O hidrogel não adere a plaquetas no sangue, não causa trombose e não tem nada tóxico em sua solução”, explica Faria. Nessa cápsula é inserido um polímero condutor – metal sintético que conduz cargas elétricas – que, de acordo com sua intensidade, muda de cor e tamanho. É esse polímero que dá a coloração preta ao sistema. “Como o hidrogel é muito poroso, o polímero condutor cresce e permeia o material, formando uma camada de revestimento em seus poros, tudo em escala nanométrica”, afirma Faria. Após a aplicação do polímero, o sistema é mergulhado em uma solução com o medicamento desejado. O sistema age como uma esponja, absorvendo o medicamento por difusão. O que permite o controle na liberação dessa droga é o contato elétrico do polímero com uma fonte de energia, seja uma pequena bateria ou um chip. “Daí nós lançamos um sinal para o polímero, que se expande e contrai, aumentando ou diminuindo o tamanho do revestimento do poro do hidrogel e assim liberando o medicamento que está lá dentro”, relata Faria. Como esse sinal elétrico pode ser controlado automaticamente, o paciente recebe sempre a dose adequada do medicamento, mantendo o nível deste no sangue sempre acima do mínimo para ser efetivo e abaixo do máximo, quando pode se tornar tóxico (veja gráfico nesta página). “É como um soro de hospital, em que as gotas caem sempre a uma velocidade determinada para que o nível do medicamento se mantenha adequado ao paciente. Mas, com esse aplicativo em miniatura, o paciente não precisa ficar deitado na cama nem ter uma enfermeira sempre controlando o soro”, propõe Faria.
Aplicativo multiuso – Os sistemas de liberação controlada de medicamento já são conhecidos no mercado, principalmente pelas mulheres, que utilizam desde adesivos cutâneos até dispositivos intra-uterinos, para aplicação de anticoncepcionais por tempo prolongado. Mesmo o hidrogel já é utilizado desde 1960, em sistemas de liberação controlada para insulina. A diferença do novo sistema concebido por Faria é sua versatilidade de uso e seu baixo custo de produção. “Os sistemas que existem no mercado funcionam apenas com uma velocidade de liberação já programada. Este pode tanto funcionar assim como ser ajustado de acordo com o organismo de cada paciente, liberando mais droga quando for preciso e interrompendo a liberação quando não for necessário”, ressalta. Apesar de ter sido produzido em pequenas cápsulas para aplicação subcutânea, o sistema pode ser produzido em qualquer tamanho, de acordo com a dose do medicamento e o tempo de duração do tratamento. Sua estrutura permite ainda a aplicação de qualquer droga, ao contrário dos sistemas já encontrados no mercado, que só funcionam com insulina. “Como é primordialmente um sistema de liberação de moléculas, poderia ser utilizado até em outras áreas, como dispositivo de liberação de agrotóxicos em plantações de forma controlada ou mesmo para aplicação de essências”, afirma Faria. O pesquisador também propõe a acoplagem do seu sistema químico a um biossensor que, aplicado no organismo, reconhece o momento necessário para a liberação do medicamento. “Esse uso pode ser muito útil no caso da diabete, já que a aplicação da insulina depende do nível de glicose no sangue. Um biossensor de glicose, como os que já existem no mercado, pode ser acoplado ao sistema liberando a insulina de acordo com o nível da substância no organismo do paciente”, explica Faria. Com a possibilidade de diversos usos, Faria não tem dúvidas de que seu sistema terá espaço garantido no mercado. Segundo ele, grande parte dos investimentos da indústria farmacêutica está concentrada em sistemas de liberação controlada. “Nesta era de genéricos, a fórmula do medicamento não é mais um diferencial. A novidade está no meio de aplicá-la no organismo. Por isso vejo uma grande possibilidade de retorno financeiro ao nosso laboratório e à USP com esta invenção”, prevê. Com uma novidade promissora em mãos, Faria busca agora patenteá-la para defender sua descoberta e garantir os direitos sobre sua comercialização. “A união desses materiais neste sistema é inédito e não queremos perder a posse desta invenção, que é fruto de árduo trabalho”, explica. Mas, antes de chegar às farmácias, o aplicativo tem de passar por diversas etapas de teste, inclusive testes in vivo (em seres vivos) já que durante sua pesquisa foram realizados apenas testes in vitro (no laboratório). “Nós desenvolvemos a etapa inicial do sistema. Estamos cientes de que este é o caminho para que outros pesquisadores se interessem pelo projeto e o levem adiante, seja fazendo testes com outras substâncias, seja realizando os testes necessários para chegar à indústria farmacêutica”, diz Faria. O sistema foi proposto a Faria por sua orientadora, a professora
Susana Córdoba Torresi, do Instituto de Química da
USP. “Eu ia fazer um estudo em outra área, algo que
já vinha desenvolvendo na minha iniciação
científica. A professora Susana me deu um artigo falando
sobre o assunto e propôs uma pesquisa que abriria novos caminhos
no laboratório, e eu aceitei.”
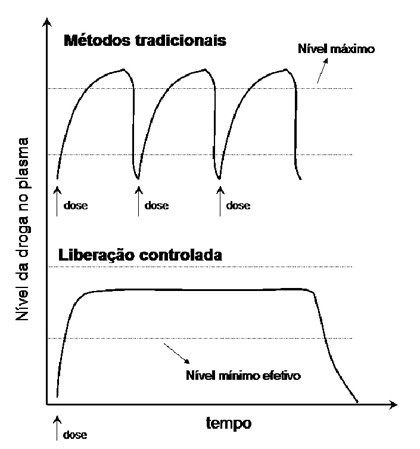
No gráfico acima, vê-se a diferença entre os métodos convencionais de aplicação de medicamento, como vacinas e pílulas, e o novo sistema projetado pelo pesquisador Luiz Marcos de Lira Faria. No gráfico de cima, há uma grande oscilação, causada pelos métodos mais conhecidos, no qual o medicamento demora a entrar na corrente sanguínea e resulta em grandes picos no nível da droga no sangue a cada dose tomada. Já no gráfico de baixo, o método de aplicação controlado através de sinais elétricos resulta em uma constante liberação da droga no sangue e, conseqüentemente, produz estabilidade no nível de medicamento e maior tempo de ação do tratamento. “Este sistema foi elaborado para que o paciente mantenha sempre um nível adequado do medicamento no sangue e com isso possa tomar o mínimo de doses possível. Isso facilita a vida de todo paciente e garante que haja também o mínimo possível de efeitos colaterais”, explica Faria.
|
O Jornal da USP é um órgão da Universidade de São Paulo, publicado pela Divisão de Mídias Impressas da Coordenadoria de Comunicação Social da USP.
[EXPEDIENTE] [EMAIL]